Enlace Pi
Es un enlace covalente formado por la hibridación de dos orbitales atómicos p. Los orbitales d también pueden participar en este tipo de enlace.
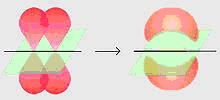

El enlace sigma es uno de los enlaces más fuertes, con mayor estabilidad. La densidad electrónica se dispone de manera simétrica entre los núcleos de los átomos, como se ve en la figura de arriba.
Según los orbitales que se hayan hibridado para formar el enlace sigma, éste tipo de enlace se puede clasificar en:
Enlace sigma s. Es el formado por la hibridación de dos orbitales s.

Enlace sigma sp. Formado por la hibridación de un orbital s y uno p.

Enlace sigma p. Se obtiene cuando se traslapan dos orbitales p en sentido longitudinal.

Según la estabilidad química los enlaces pueden ser sigma (σ) o pi(π), en forma practica estos enlaces se reconocen así:
Referencias:
-Química en la guía 2000. http://quimica.laguia2000.com/general/enlace-pi
-Química en la guía 2000. http://quimica.laguia2000.com/conceptos-basicos/enlace-sigma
-Fullquímica. http://www.fullquimica.com/2011/04/enlace-covalente.html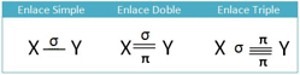
No hay comentarios:
Publicar un comentario